Obsah
Aj keď všetky atómy toho istého prvku obsahujú rovnaký počet protónov, počet neutrónov sa môže meniť. Vedieť, koľko neutrónov má konkrétny atóm, vám môže pomôcť určiť, či je častica pravidelná v tomto prvku alebo v izotope, ktorý bude mať viac alebo menej neutrónov. Stanovenie počtu neutrónov v atóme je pomerne jednoduché a nevyžaduje žiadny experiment. Ak chcete vypočítať počet neutrónov v bežnom atóme alebo izotope, postupujte podľa týchto pokynov spolu s periodickou tabuľkou.
kroky
Metóda 1 z 2: Nájdenie počtu neutrónov v spoločnom atóme
Vyhľadajte prvok v periodickej tabuľke. V tomto príklade sa pozrime na OS (OS), ktorý je v šiestom riadku, zhora nadol.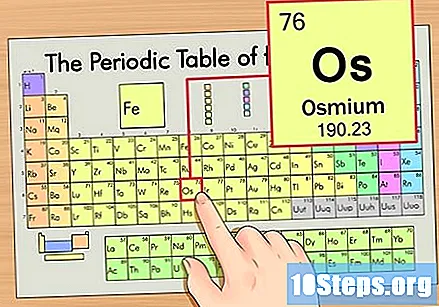
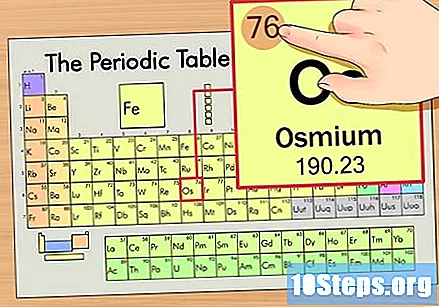
Nájdite atómové číslo prvku. Toto je zvyčajne najviac viditeľné číslo pre konkrétny prvok a je zvyčajne nad jeho symbolom (v tabuľke, ktorú používame, v skutočnosti nie je uvedené žiadne iné číslo). Atómové číslo je počet protónov v jednom atóme tohto prvku, Počet Os je 76, čo znamená, že atóm Osmium má 76 protónov.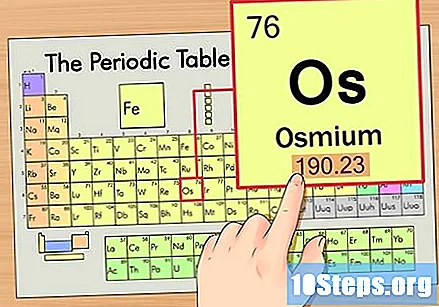
Nájdite atómovú hmotnosť prvku. Toto číslo sa zvyčajne nachádza pod atómovým symbolom. Všimnite si, že tabuľka v tomto príklade je založená iba na atómovom čísle a neuvádza atómovú hmotnosť. To nebude vždy tak. Osmium má atómovú hmotnosť 190,23.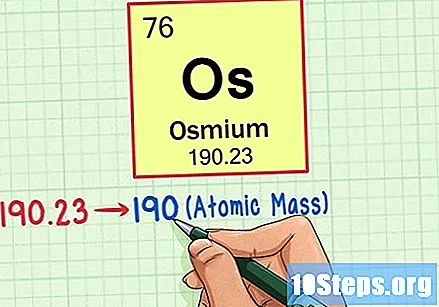
Zaokrúhlite atómovú hmotnosť na najbližšie celé číslo, aby ste našli atómovú hmotnosť. V našom príklade by bolo 190,23 zaokrúhlené na 190, čo by viedlo k atómovej hmotnosti 190 pre Osmium.- Atómová hmotnosť je priemer izotopov prvku. Preto to zvyčajne nie je celé číslo.
Odčítajte atómové číslo od atómovej hmotnosti. Pretože drvivá väčšina atómovej hmoty sa nachádza v jej protónoch a neutráloch, odpočítaním počtu protónov (tj atómového čísla) od atómovej hmotnosti získate číslo počítané neutrónov v atóme. Číslo za desatinnou čiarkou všeobecne predstavuje veľmi malú hmotnosť elektrónov v atóme. V našom príklade je to: 190 (atómová hmotnosť) - 76 (počet protónov) = 114 (počet neutrónov).
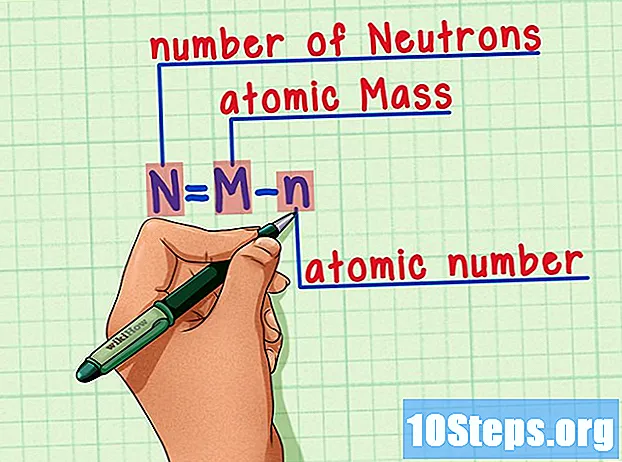
Pamätajte na vzorec. Ak chcete zistiť počet neutrónov v budúcnosti, použite tento vzorec: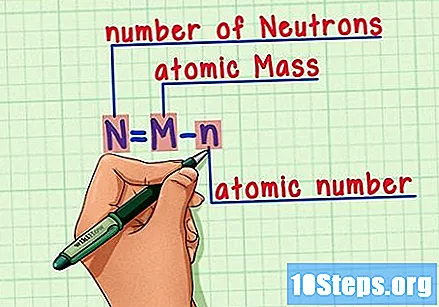
- N = M - n.
- N = počet Neutrons.
- M = Matómová pečeň.
- n = natómový humerus.
- N = M - n.
Metóda 2 z 2: Nájdenie počtu neutrónov v izotope
Vyhľadajte prvok v periodickej tabuľke. Použime napríklad izotop uhlíka-14. Pretože neizotopická forma uhlíka-14 je jednoducho uhlík (C), nájdite tento prvok v periodickej tabuľke (v druhom riadku).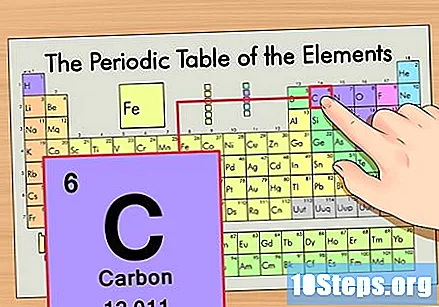
Nájdite atómové číslo prvku. Toto je zvyčajne najviac viditeľné číslo pre konkrétny prvok a je zvyčajne nad jeho symbolom (v tabuľke, ktorú používame, v skutočnosti nie je uvedené žiadne iné číslo). Atómové číslo je počet protónov v jednom atóme tohto prvku, C je číslo 6, čo znamená, že atóm uhlíka má 6 protónov.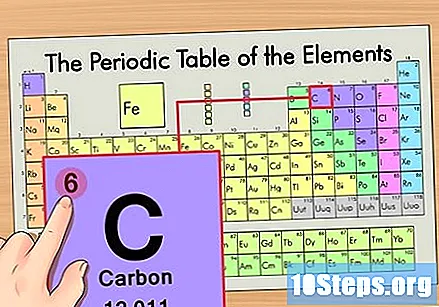
Nájdite atómovú hmotnosť. U izotopov je to neuveriteľne ľahké, pretože sú pomenované podľa atómovej hmotnosti. Uhlík-14 má atómovú hmotnosť 14. Akonáhle nájdete atómovú hmotnosť izotopu, proces zisťovania počtu neutrónov je rovnaký ako v prípade bežných atómov.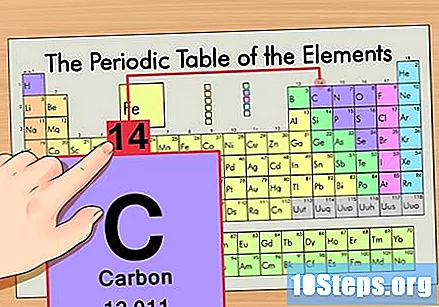
Odčítajte atómové číslo od atómovej hmotnosti. Pretože drvivá väčšina atómovej hmoty sa nachádza v jej protónoch a neutráloch, odpočítaním počtu protónov (tj atómového čísla) od atómovej hmotnosti získate číslo počítané neutrónov v atóme. Číslo za desatinnou čiarkou všeobecne predstavuje veľmi malú hmotnosť elektrónov v atóme. V našom príklade je to: 14 (atómová hmotnosť) - 6 (počet protónov) = 8 (počet neutrónov).
Pamätajte na vzorec. Ak chcete zistiť počet neutrónov v budúcnosti, použite tento vzorec: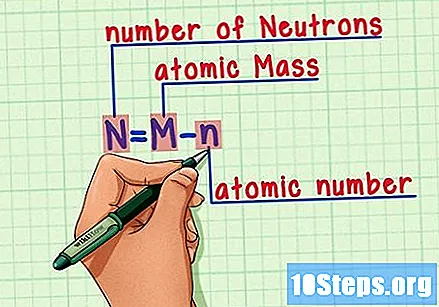
- N = M - n.
- N = počet Neutrons.
- M = Matómová pečeň.
- n = natómový humerus.
- N = M - n.
Tipy
- Osmium, pevný kov pri izbovej teplote, odvodzuje svoj názov z gréckeho slova „zápach“, „osme“.
- Protóny a neutróny tvoria takmer celú hmotnosť prvkov, zatiaľ čo elektróny a iné rôzne častice predstavujú zanedbateľnú hmotu (blížiaca sa k nulovej hmotnosti). Pretože protón má približne rovnakú hmotnosť ako neutrál a atómové číslo predstavuje počet protónov, môžeme jednoducho odpočítať počet protónov od celkovej hmotnosti.
- Ak si nie ste istí, ktoré číslo je v periodickej tabuľke, nezabudnite, že sa zvyčajne vytvára okolo atómového čísla (tj počtu protónov), ktoré začína číslom 1 (vodík) a zvyšuje sa o jednu jednotku na zľava doprava, končiaca na 118 (Ununóctio). Je to tak preto, že počet protónov v atóme určuje, čo je tento atóm, čím uľahčuje organizovanie elementárnej charakteristiky (napríklad atóm s 2 protónmi bude vždy hélium, rovnako ako ďalší atóm so 79 protónmi bude vždy zlato).


