Obsah
- stupňa
- Metóda 1 Vyrovnanie rovnice metódou pokusov a omylov
- Metóda 2 Rovnováhu rovnice algebraickou metódou
V chémii určuje rovnica, čo sa stalo počas chemickej reakcie. Naľavo od rovnice umiestnime reagencie, ktoré sa použili na experiment, a napravo produkty získané počas experimentu. Podľa princípu zachovania hmoty (Lavoisier) počas chemickej reakcie žiadny atóm nezmizne, žiaden sa nevytvorí, kombinujú sa inak. V súhrne musíte mať rovnaké číselné údaje každého prvku napravo ako naľavo od rovnice. Preto musí byť rovnovážna rovnica vždy vyvážená.
stupňa
Metóda 1 Vyrovnanie rovnice metódou pokusov a omylov
-
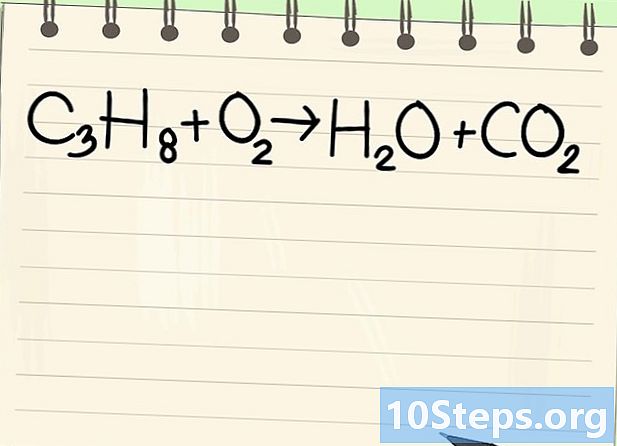
Všimnite si rovnovážnej rovnice. Budeme sa zaoberať nasledujúcou rovnicou:- C3H8 + O2 -> H2O + CO2
- Toto je rovnica spaľovania propánu (C3H8) v kyslíku: získajú sa voda a oxid uhličitý.
-
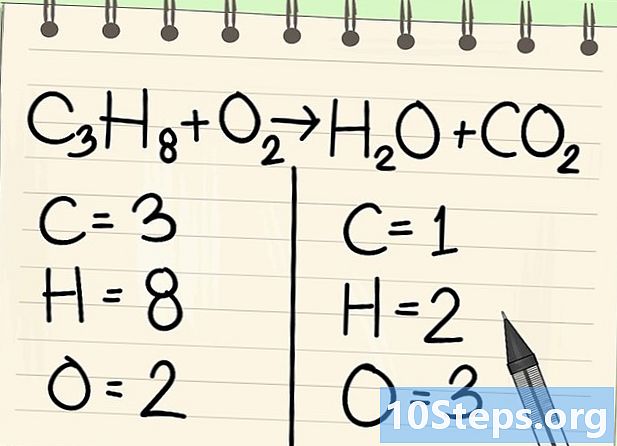
Počítajte atómy. Zadajte počet údajov každého prvku na jednej strane rovnice a potom na druhý. Zohľadnite preto indexy, ak neexistujú, index je 1.- Vľavo sú 3 atómy uhlíka, 8 vodíka a 2 kyslíky.
- Vpravo je 1 atóm uhlíka, 2 vodík a 3 kyslík.
-
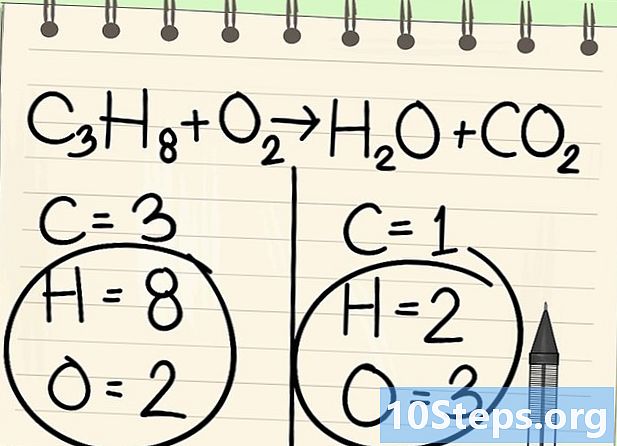
Na chvíľu nechajte vodík a kyslík. -

Začnite vyvážiť správnym prvkom. Vždy začíname s jednou v molekule pred a po reakcii. Ak je ich niekoľko, zoberte ten, ktorý je monovalentný v jednej z molekúl. Tu začíname atómami uhlíka. -

Vyvážte atómy uhlíka. Napravo pridajte koeficient k molekule oxidu uhličitého (CO2), v ktorom je uhlíkový latóm samotný. Dáme 3, aby sme dostali 3 zvyšné atómy.- C3H8 + O2 -> H2O + 3CO2
- Vďaka koeficientu (3CO) máme teda vpravo 3 uhlíkové atómy2) a 3 uhlíkové atómy vľavo vďaka indexu (C3H8).
- V rovnici môžete vložiť všetky požadované koeficienty, ale nemôžete sa dotknúť vodítka.
-
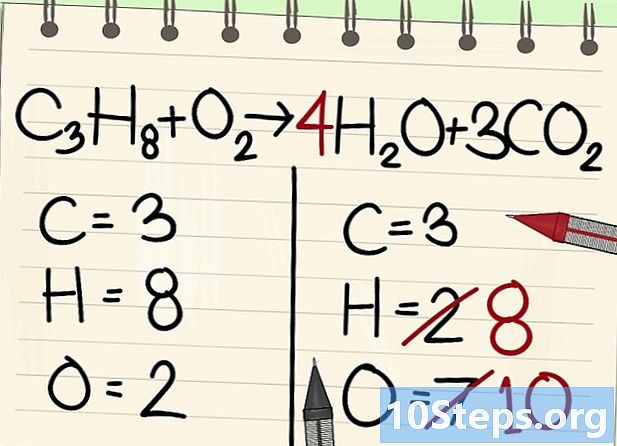
Vyvážte atómy vodíka. Keď už máte 8 rovníc, potrebujete toľko pravdy.- C3H8 + O2 --> 4H2O + 3CO2
- Vpravo dáte koeficient 4, pretože vodík je v molekule vody dvojmocný: index 2 znamená, že sú spojené dva atómy vodíka.
- Ak chcete získať počet atómov vodíka vpravo, vynásobte koeficient 4 indexom 2 alebo 8 atómami.
- Pokiaľ ide o atómy kyslíka, na pravej strane je teraz 6 na jednej strane, ktoré pochádzajú z troch molekúl 3CO2 (3 x 2 = 6 atómov) a 4 zo 4 molekúl 4H2O (4 x 1 = 4 atómy), tj celkom 10 atómov kyslíka.
-
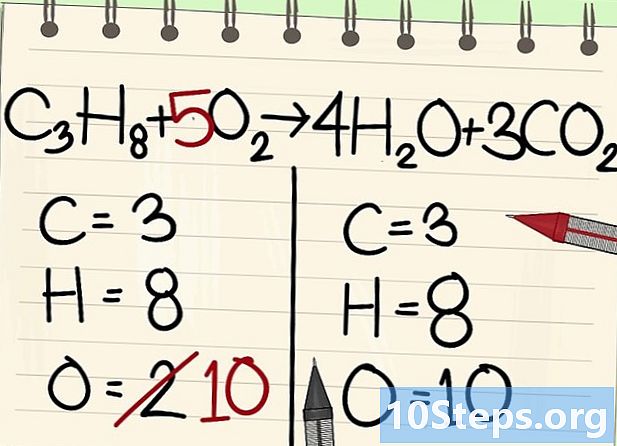
Vyvážte atómy kyslíka.- Z dôvodu uhlíkovej a vodíkovej rovnováhy nie je počet atómov kyslíka na oboch stranách rovnice rovnaký. Už sme predtým videli, že napravo je 10 atómov kyslíka (4 z molekúl vody a 6 z molekúl oxidu uhličitého). Vľavo sú iba 2 (od O2).
- Na vyrovnanie kyslíka pridajte k ľavej molekule kyslíka koeficient 5: vľavo máte 10 atómov kyslíka a ostatné vpravo.
- C3H8 + 5O2 -> 4H2O + 3CO2
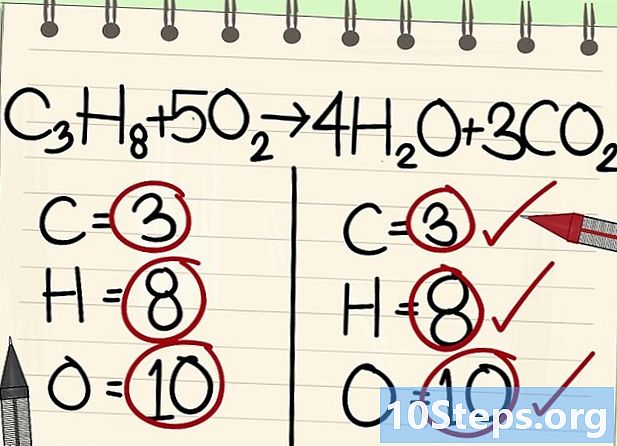
- Všetky atómy (uhlík, vodík a kyslík) sú vyvážené: vaša rovnica je vyrovnaná.
Metóda 2 Rovnováhu rovnice algebraickou metódou
-

Napíšte rovnicu do rovnováhy. Každej molekule priraďte literálny koeficient. Zavoláme im má, b, C a d. -
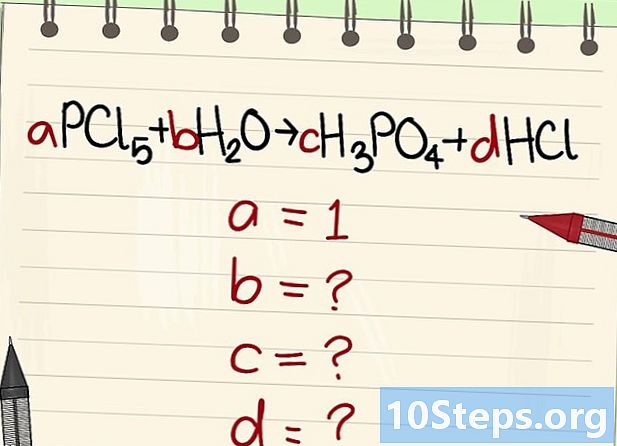
Nájdite hodnotu ostatných literálových koeficientov. Budeme sa pýtať má = 1. -

Nájdite vzťahy medzi týmito koeficientmi. Pri pohľade doľava (reagenty) a vpravo (produkty) stanovte vzťahy medzi týmito rôznymi koeficientmi.- Vezmite nasledujúcu rovnicu: aPCl5 + bH20 = cH3P04 + dHCl. Bolo uvedené, že a = 1, čo znamená, že c = a, d = 5a a 2b = 3c + d. Uskutočnené výpočty, c = 1, d = 5 ab = 4.

- Vezmite nasledujúcu rovnicu: aPCl5 + bH20 = cH3P04 + dHCl. Bolo uvedené, že a = 1, čo znamená, že c = a, d = 5a a 2b = 3c + d. Uskutočnené výpočty, c = 1, d = 5 ab = 4.