Obsah
Ostatné oddielyVodík je najľahší prvok a má mnoho priemyselných využití, vrátane tvorby hydrogenovaných tukov používaných v kuchyni a výroby uhľovodíkov z uhlia. Je nevyhnutnou súčasťou molekúl vody a dá sa oddeliť pomocou malého množstva elektriny. Plynný vodík môžete vyrábať aj pomocou niektorých aktívnych kovov a silných kyselín. Obidve metódy sú pomerne jednoduché a umožnia vám zhromaždiť plynný vodík.
Kroky
Metóda 1 z 2: Použitie výtlaku vody s aktívnymi kovmi
Zhromaždite potrebné materiály. Na zachytávanie vodíka reakciou zmiešania silnej kyseliny s aktívnym kovom budete potrebovať: Erlenmeyerovu banku, gumenú zátku, plastové hadičky, destilovanú vodu, skúmavky, veľkú nádobu, 3 molárnu kyselinu chlorovodíkovú (HCl) a horčíkové alebo zinkové pelety.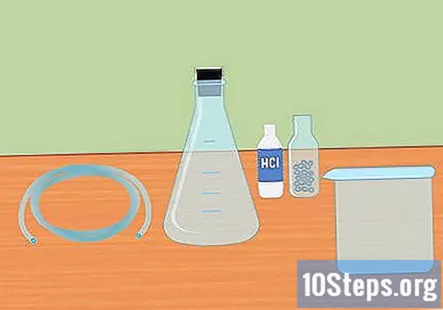
- Erlenmeyerova banka je sklenená banka, ktorá má kónické dno a valcovité hrdlo.
- Gumová zátka je pre hornú časť banky a musí mať v strede otvor, aby mohla prejsť hadička.
- Pri tomto experimente bude fungovať buď horčík alebo zinok, nepotrebujete oboje.
- Možno bude potrebné kúpiť niektoré z týchto spotrebných materiálov online alebo v obchode s laboratórnymi potrebami.

Noste vhodné ochranné vybavenie. Pri práci so silnou kyselinou, ako je kyselina chlorovodíková, sa musíte ubezpečiť, že dodržiavate správne bezpečnostné opatrenia. Noste laboratórny plášť, rukavice, obuv s uzavretými prstami a ochranu očí.- Okuliare by sa mali zabaľovať okolo očí, aby boli chránené pred postriekaním.
- Noste rukavice, ktoré sedia správne, aby ste si zachovali dobrú šikovnosť svojich rúk a prstov.
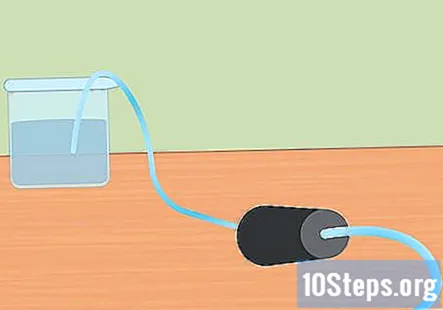
Pripravte experimentálne nastavenie. Vložte jeden koniec hadičky do otvoru gumovej zátky. Chcete, aby hadica prešla úplne cez gumovú zátku a aby mierne trčala od konca. Naplňte veľkú nádobu vodou a vložte voľný koniec hadičky do vody. Na začiatku experimentu vložíte gumovú zátku do Erlenmeyerovej banky.- Tieto kúsky odložte, kým nebudete pripravení ich použiť.
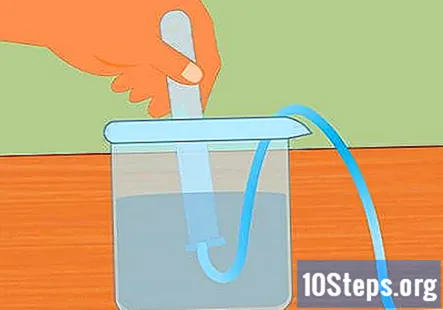
Ponorte skúmavku do vody. Vezmite aspoň jednu skúmavku (môžete použiť viac, ak chcete zhromaždiť viac vodíka) a ponorte ju do vody. Sklopte hadičku tak, aby mohli unikať všetky vzduchové bubliny. Hadičku umiestnite na hornú časť ponorenej hadičky pripevnenej k gumovej zátke na opačnom konci.- Je nevyhnutné, aby ste z trubice odstránili všetky vzduchové bubliny skôr, ako začnete. Ak nie sú, plyn zhromaždený v trubici bude viac než len vodík.
Do Erlenmeyerovej banky sa pridá kyselina chlorovodíková. Pridajte toľko kyseliny chlorovodíkovej, aby bola banka naplnená asi do polovice. Malo by stačiť asi 100 ml. Pred pridaním kyseliny sa uistite, že je banka čistá a suchá. Noste gumené rukavice a pri plnení banky buďte opatrní.
- Dajte pozor, aby ste na kyselinu nevyliali žiadnu vodu. Voda pridaná do kyseliny môže viesť k výbuchu a zraneniu.
Chemickú reakciu spustite pridaním kovových peliet do HCl. Do kyseliny chlorovodíkovej v banke pridajte niekoľko zinkových alebo horčíkových peliet. Presné množstvo, ktoré vložíte, nie je dôležité, na spustenie reakcie by vám však mala stačiť malá hrsť.
- Po pridaní peliet vložte zátku do banky tak, aby bol systém teraz uzavretý.
Vodík sa zachytáva v ponorenej skúmavke. Keď kov reaguje s kyselinou, vzniká plynný vodík. Tento vodík putuje do hornej časti banky cez hadičky a do skúmavky ponorenej vo vode. Plyn vytlačí vodu a v hornej časti skúmavky by ste mali vidieť bublinu.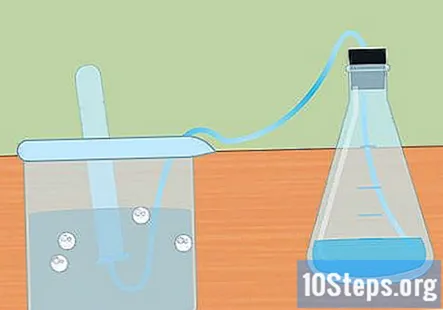
- Keď je skúmavka naplnená vodíkom, ponorte ďalšiu skúmavku do vody a položte ju na hadičky. Môžete zhromaždiť toľko vodíka, koľko vyprodukuje vaša reakcia.
- Skúmavky držte smerom nadol, aby plynný vodík neunikal do vzduchu.
Potvrďte, že plyn je vodík. Aby ste potvrdili, že plyn je vodík, môžete urobiť takzvaný test dlahy. Zapáľte zápalku a podržte ju pod trubičkou. Budete počuť praskanie alebo škrípanie, ktoré naznačuje, že je prítomný vodík.
Metóda 2 z 2: Použitie elektrolýzy
Zhromaždite potrebné materiály. V tomto experimente budete pomocou elektriny oddeľovať plyny vodíka a kyslíka od molekúl vody. Na zber plynného vodíka pomocou elektrolýzy budete potrebovať 9-voltovú batériu, ceruzku, dve skúmavky, plastovú nádobu, vodu, sódu bikarbónu, dve veľké gumičky (voliteľné) a svorku na batériu so svorkami na konci.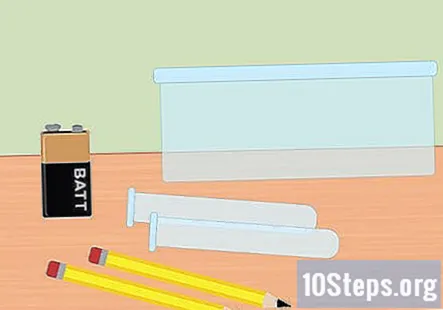
- Aby to fungovalo, musí mať ceruzka v sebe grafit. Ceruzka číslo 2 je perfektná. K tomu budú fungovať aj dva malé kúsky grafitu.
- Postačí malá nádoba alebo miska na skladovanie potravín.
- Uistite sa, že do svorky na batériu sa zmestí 9-voltová batéria a že má červený a čierny drôt s krokosvorkami na konci. Tieto svorky sa použijú na pripojenie vášho systému k batérii.
Vyberte gumu z ceruzky a rozlomte ju na polovicu. Potrebujete dva kusy grafitu, jeden pre kladný koniec batérie a pre záporný koniec batérie. Naostrite obidva konce každého kúska ceruzky na bod. Uistite sa, že grafit je dobre exponovaný.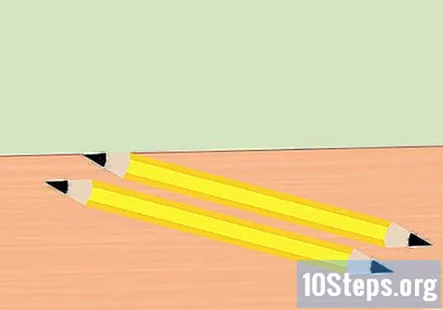
- Tento krok je možné preskočiť, ak už máte dva kusy čistého grafitu.
Omotajte 2 gumičky okolo nádoby v tvare X. Tento krok je voliteľný, ale predstavuje jednoduchý spôsob, ako udržať skúmavky na mieste, aj keď je experiment v prevádzke. Napnite jednu gumičku na nádobu a natiahnite na ňu druhú gumičku tak, aby prechádzala cez prvú a tvorila X.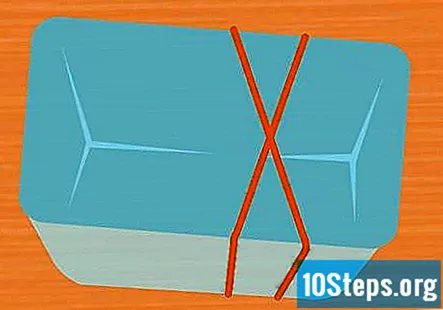
- Ak nepoužívate gumičky, nezabudnite skúmavky zaistiť páskou alebo šnúrkou tak, aby počas experimentu zostali hore nohami.
Pripravte sódu bikarbónu a vodný roztok. Rozpustenie sódy bikarbóny vo vode pomôže elektrine v systéme. Presné množstvo pridanej sódy bikarbóny nie je dôležité, ale malo by stačiť asi 1 čajová lyžička na 1 pohár vody. Miešajte, kým sa úplne nerozpustí.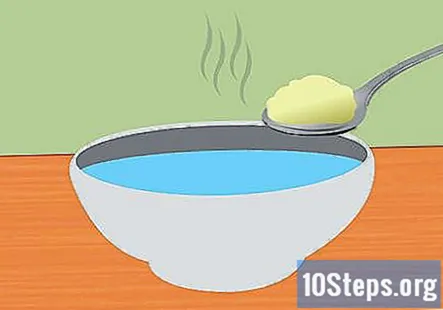
- Na urýchlenie rozpúšťania sódy bikarbóny použite teplú vodu.
Naplňte plastovú nádobu a skúmavky roztokom sódy bikarbóny. Nádoba musí byť dostatočne veľká, aby pojala obe skúmavky. Pridajte dostatok roztoku, aby ste nádobu naplnili asi do troch štvrtín. Ponorte skúmavky do roztoku nádoby a vyklopte ich dnom hore. Každú hadičku vložte do kríža gumičky X, aby ste ju držali na danom mieste.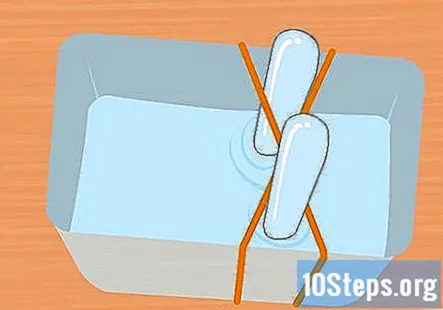
- Je veľmi dôležité, aby obe skúmavky boli úplne plné vody a nezostali žiadne vzduchové bubliny.
Pripojte aligátorové svorky k grafitu. Vyberte jednu svorku zo svorky na batériu a pripevnite ju na koniec jednej z ceruziek. Uistite sa, že sa dotýka čo najväčšej časti grafitu. To isté urobte so zostávajúcou aligátorovou svorkou a kúskom ceruzky.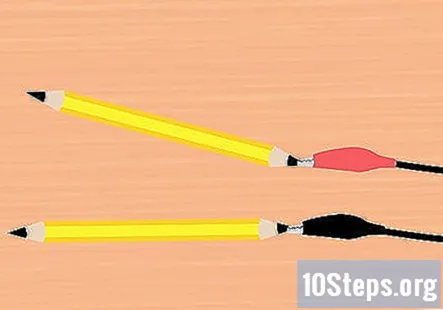
- Jedna ceruzka by mala byť pripevnená k červenej svorke a jedna ceruzka k čiernej svorke.
Nezasunutý koniec ceruzky zasuňte do skúmavky. Udržujte skúmavku úplne ponorenú a mierne ju nakloňte, aby ste mohli zasunúť nezviazaný koniec ceruzky do skúmavky. Tento postup opakujte s druhou ceruzkou a druhou skúmavkou.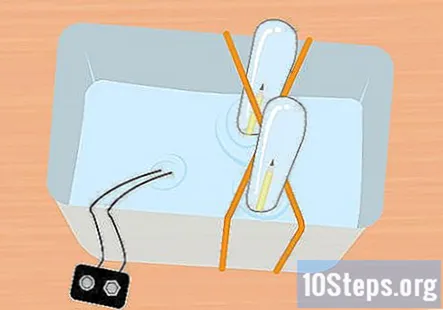
- V tomto okamihu by malo byť všetko pod vodou a vo vnútri každej skúmavky by mal byť jeden kúsok ceruzky.
- Koniec svorky batérie, ktorý sa pripája k batérii, udržujte mimo vody.
Pripojte sponu batérie k 9-voltovej batérii. Keď je všetko pripravené, ste teraz pripravení používať elektrinu poskytovanú 9-voltovou batériou. Koniec spony batérie by mal vyčnievať z nádoby, takže batériu jednoducho zafixujte na danom mieste. Akonáhle je batéria pripojená, mali by ste si všimnúť bubliny stúpajúce od konca grafitu a plávajúce k hornej časti každej skúmavky.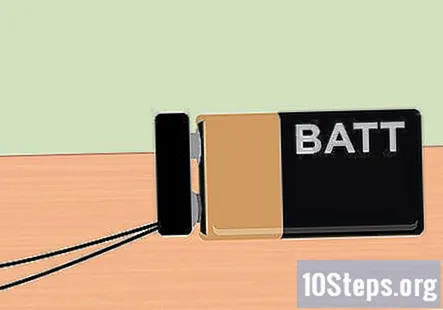
- Ak nevidíte vytváranie bublín, skontrolujte, či sú svorky aligátora pevne spojené s grafitom ceruzky. Skontrolujte tiež, či je batéria úplne nabitá.
- Skúmavka so záporným vodičom pripojeným k ceruzke bude vyrábať vodík, zatiaľ čo skúmavka pripojená k kladnému vodiču batérie bude produkovať kyslík.
Zhromažďujte vodík a kyslík v dvoch skúmavkách, kým v každej skúmavke nezostane niekoľko centimetrov plynu. Pamätajte, že trubica pripojená k zápornému koncu batérie bude obsahovať vodík a kyslík bude v trubici pripojenej k kladnému koncu. Skúšobné skúmavky vyberte z banky po jednom. Držte ich hore dnom a nechajte odtekať vodu. Plyn v skúmavkách zostane, aj keď ho nevidíte.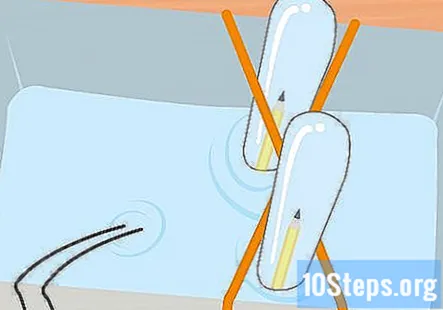
Skúška na prítomnosť vodíka. Prítomnosť vodíka môžete otestovať štrajkom a držaním plameňa až po plyn. Ak je to vodík, vydá veľmi zreteľný „piskľavý pop“ zvuk. Namiesto zápalky môžete použiť aj zapálenú sviečku.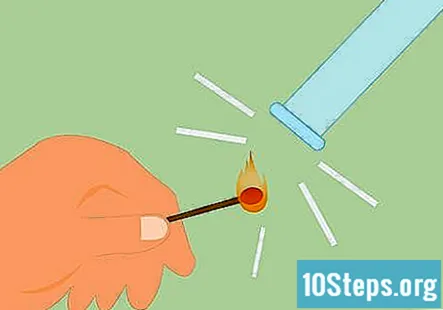
- Ak chcete testovať obsah kyslíka v skúmavke, ktorá bola pripojená k pozitívnej strane zdroja energie, vyfúknite zapálenú zápalku (alebo sviečku) a vložte stále žiariaci koniec pod skúmavku. Ak sviečka znovu zapáli, je prítomný kyslík.
Otázky a odpovede pre komunitu
Potrebujem dve skúmavky, ak chcem zhromažďovať iba vodík?

Vedkyňa pre životné prostredie Bess Ruff je doktorandkou z geografie na Floridskej štátnej univerzite. V roku 2016 získala magisterský titul v odbore environmentálna veda a manažment na Kalifornskej univerzite v Santa Barbare. Vykonávala prieskumné práce pre projekty morského priestorového plánovania v Karibiku a poskytovala podporu výskumu ako absolventka skupiny pre trvalo udržateľný rybolov.

Koľko vodíka sa dá zhromaždiť z tohto jednoduchého experimentu elektrolýzy? A aký by bol tlak plynného vodíka?
To záleží. Rýchlosť reakcie (štiepenie vody) závisí od zosilnenia batérie a času zostávajúceho do reakcie. Vodík by bol typicky asi na úrovni tlaku mora, pokiaľ experiment neuskutočníte v skutočne teplom alebo studenom prostredí.
Prečo sa vodík zhromažďuje v negatívnej trubici
Vďaka spôsobu, akým molekuly vody zdieľajú elektróny, sú atómy vodíka pozitívne nabité a atómy kyslíka negatívne nabité. Pri odťahovaní plynov bude pozitívne nabitý vodík priťahovaný k negatívnej trubici, zatiaľ čo negatívne nabitý kyslík bude priťahovaný k pozitívnej trubici.
Prečo plyn neunikal z mojej trubice na zhromažďovanie plynu?
Je to vodík, plyn, ktorý je ľahší ako všetky ostatné, vrátane hélia, čo znamená, že zostane v skúmavke, pokiaľ je na nej uzavretý koniec, pretože ho vylučujú ostatné plyny. Dôvod, prečo používame hélium namiesto vodíka, je ten, že nie je horľavý. Je to spôsobené tým, že ide o vzácny plyn (má plnú valenčnú vrstvu 8 elektrónov), a preto je nereaktívny.
Bol by plyn veľmi horľavý?
Áno. Pozri si katastrofu Hindenburg na YouTube. Zeppelíny používali vodík, pretože to bol najľahší plyn a pomerne ľahko sa získaval. Aj preto niektorí výrobcovia automobilov pracujú na autách na vodíkový pohon.
je to tekutá forma vodíka?
Nie - vodík v tomto experimente bude plynný
Ako skvapalním vodík? Odpoveď
Varovania
- S čistým vodíkom buďte opatrní. Pri zmiešaní so vzduchom je vysoko výbušný.
- Zaistite, aby bol zo zariadenia, v ktorom zhromažďujete vodík, odstránený všetok ostatný vzduch.


